- · 《临床药物治疗杂志》编[10/30]
- · 《临床药物治疗杂志》杂[10/30]
- · 《临床药物治疗杂志》杂[10/30]
- · 《临床药物治疗杂志》期[10/30]
- · 《临床药物治疗杂志》数[10/30]
- · 《临床药物治疗杂志》投[10/30]
- · 临床药物治疗杂志版面费[10/30]
【盘点】急性髓细胞白血病靶点及临床药物研究
作者:网站采编关键词:
摘要:本文系生物谷原创编译,欢迎分享,转载须授权! 目前,急性髓细胞白血病(AML)最传统的治疗方法是异源造血干细胞移植,然而依旧存在术后复发的几率。化疗和放疗虽对AML产生明显抑制
本文系生物谷原创编译,欢迎分享,转载须授权!
目前,急性髓细胞白血病(AML)最传统的治疗方法是异源造血干细胞移植,然而依旧存在术后复发的几率。化疗和放疗虽对AML产生明显抑制作用,但因副作用强、易复发而影响临床顺应性。免疫疗法的出现,则对复发型或者难治型AML患者而言,无疑是一种全新选择。目前,针对AML的免疫疗法药物分类主要包括以下5种:1.抗体药物偶联(ADC); 2. 双特异性 T 细胞单链抗体(Bispecific T cell engager, BiTE);3. 嵌合型抗原受体T细胞(CAR-T)疗法;4. 检查点抑制剂(Checkpoint inhibitors);5. 树突细胞疫苗(Dendritic cell vaccination)。

下面将对目前已经获批或者正在试验中的AML免疫疗法进行归纳整理:
1.抗体药物偶联(ADC)
这类生物药主要将传统细胞毒物与抗体偶联,通过抗体与抗原的特异性结合,将细胞毒物募集至肿瘤细胞处,发挥靶向杀死AML肿瘤细胞的效应。目前,抗AML ADC药物中,最主要的靶点包括CD33 (SIGLEC-3)、CD123、CD25、FLT3等。2010年,首款ADC药物吉妥单抗(gemtuzumab ozogamicin ,商品名Mylotarg,辉瑞)获得上市授权。但由于存在安全性风险,2010年FDA做出撤市决定。
除了gemtuzumab ozogamicin外,目前另三款ADC药物, SGN-CD33A (vadastuximab talirine,CD33靶点,Seattle Genetics公司)、SGN-CD123A (CD123靶点,Seattle Genetics公司)和IMGN779(CD33靶点,ImmunoGen)也顺利进入了临床试验,下面将对ADC型AML药物抗原靶点和相应药物临床情况做一汇总:
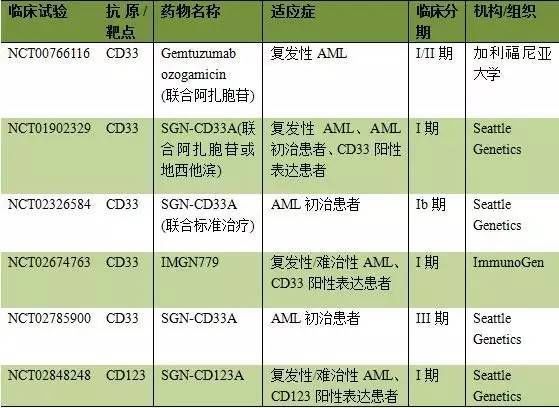
2. 双特异性 T 细胞单链抗体(bispecific T cell engager, BiTE)
这一类抗体能够通过将肿瘤细胞上的通用抗原--呈递给T细胞特异性表达蛋白,进而激活免疫系统识别和杀灭肿瘤细胞。FDA于2014年批准了首款BiTE药物blinatumomab (BLINCYTO,AMGEN公司),用于治疗包括费城染色体阴性B细胞急性白血病在内的急性白血病。
目前针对急性髓细胞白血病开发的BiTE药物,T细胞特异性蛋白靶点主要集中为CD33、CD123和CLL-1等,这些药物目前已经进入临床试验阶段。
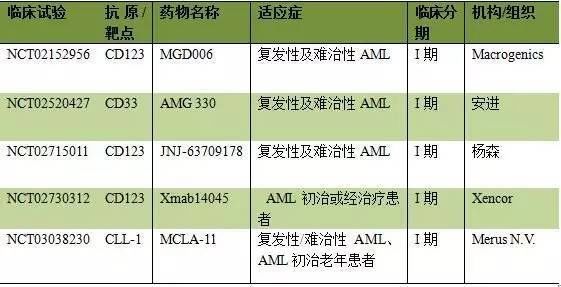
3. 嵌合型抗原受体T细胞(CAR-T)疗法
CAR-T是通过基因工程技术,人工改造肿瘤患者的T细胞,在体外大量培养后生成肿瘤特异性CAR-T细胞,再将其回输入患者体内用以攻击癌细胞。目前,针对急性髓细胞白血病治疗的CAR-T抗原靶点主要有CD33、CD123、CD44v6、CLL1、FLT3、FRβ、LeY、NKG2D 及PR1/HLA-A2 等。与ADC 和BiTE 药物相似,CD33和CD123是目前业界较为认可的两个抗原靶点,多项体内外试验表明AML小鼠经CD33 CAR-T和CD123 CAR-T输入后,癌症得到明显缓解,生存期得到有效延长。目前基于CD33和CD123靶点的多种CAR-T疗法应用于AML仍处于临床研究阶段,其余靶点仍处于临床前研究阶段。
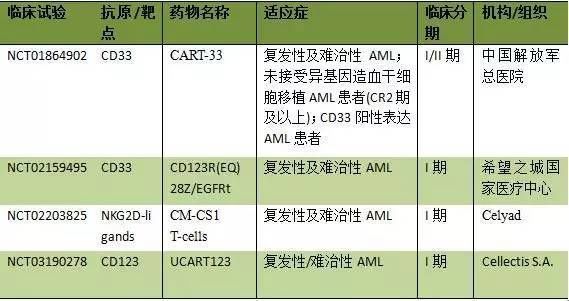
4. 检查点抑制剂
通常情况下,肿瘤细胞可产生特异性抗原,树突细胞负责吞噬凋亡肿瘤,并将肿瘤抗原呈递给T细胞。未受抑制且处于激活态的T细胞通过肿瘤特异性抗原识别并杀死肿瘤。而长时间活化的T细胞会产生PD-1和CTLA-4,并进一步诱导癌细胞产生PD-L1。PD-1与PD-L1结合,以及CTLA-4竞争性结合抗原呈递细胞(APC)表面的B7蛋白,均可以显着抑制T细胞功能,肿瘤细胞得以存活。目前AML治疗中所涉及免疫检查点抑制剂主要为CTLA-4单抗和PD-1/PD-L1单抗两种。目前尚未有这两种单抗获批用于AML治疗,但有几种已上市检查点抑制剂目前已进入临床考察阶段。
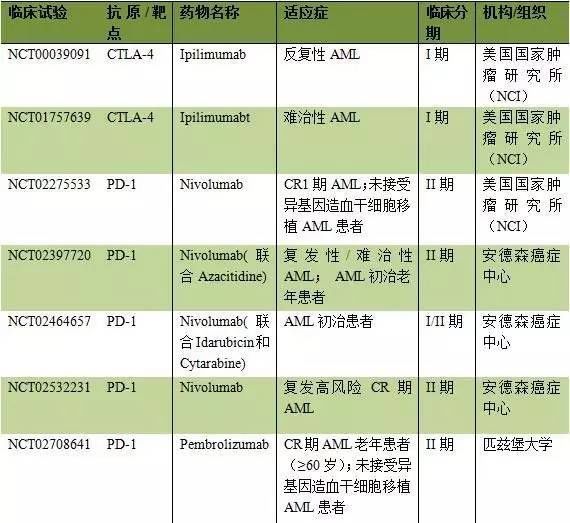
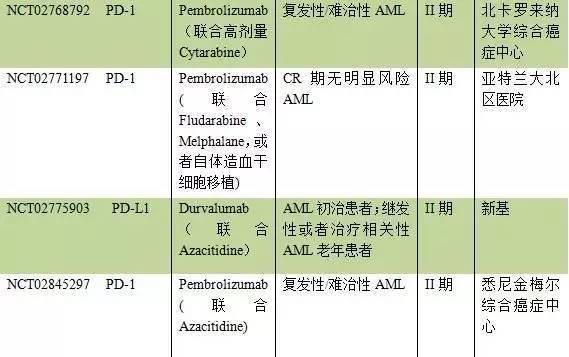
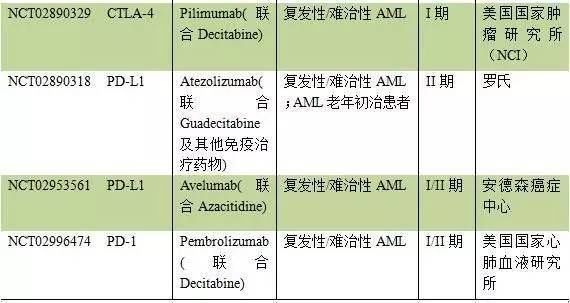
5. 树突状细胞疫苗
树突状细胞(Dendritic cell,DC)疫苗是机体免疫系统中已知的功能最强的专职抗原呈递细胞(APC),能在体内直接激活初始型T细胞。负载抗原的DC具有疫苗功能,对一些恶性肿瘤和病毒性疾病具有治疗前景。临床上应用于研究的主要是单核细胞来源的树突状细胞,目前正在进行的治疗AML的 DC疫苗研究主要有:
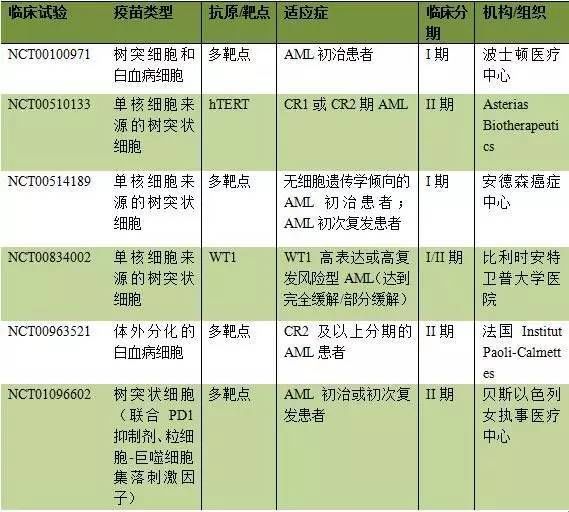
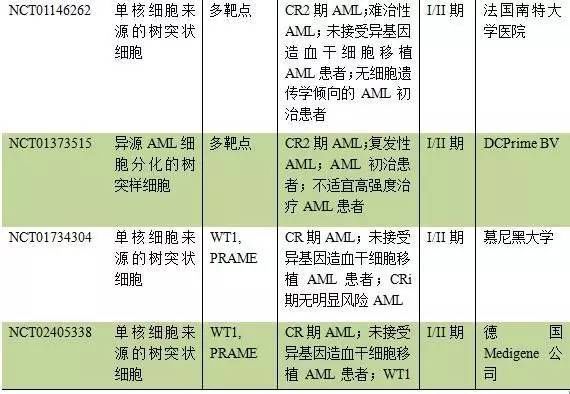
与B细胞淋巴细胞白血病(CD19 、CD20高度表达)不同,急性髓细胞白血病由于目前特异性靶点仍不明确,针对特异性靶点的疗法仍具有一定难度。因此寻找特异性治疗靶点是ADC、 BiTE和CAR-T疗法的制约瓶颈。就目前研究而言,CD33和CD123是最具前景的两个靶点,但是仍然需要更多的临床数据支持,需要更多研究人员付出努力。但愿早日实现这种个性化免疫治疗方式,降低AML的致死致残率。
文章来源:《临床药物治疗杂志》 网址: http://www.lcywzlzz.cn/zonghexinwen/2020/1103/338.html